Modelo de IA de Stanford detecta risco de 100+ doenças com uma noite de sono
SleepFM analisa uma única noite de polissonografia para prever risco futuro em mais de 100 condições. Entenda o que muda na prevenção e o que ainda falta validar.
Danilo Gato
Autor
Introdução
A palavra chave aqui é modelo de IA da Stanford. O SleepFM, publicado em 6 de janeiro de 2026 na Nature Medicine, usa dados de uma única noite de polissonografia para prever risco de mais de 100 condições, incluindo demência, Parkinson, infarto, insuficiência cardíaca e mortalidade, com índices de concordância em vários casos a partir de 0,8. É a primeira demonstração em larga escala de que o sono noturno contém assinaturas fisiológicas úteis para estratificação de risco amplo, além do diagnóstico de distúrbios do sono.
A pesquisa foi liderada por Stanford Medicine e parceiros, treinada com mais de 585 mil horas de sinais multimodais de sono de cerca de 65 mil pessoas. O estudo foi divulgado também pelo News Center de Stanford, que detalha os principais achados e a base de dados histórica usada no vínculo com prontuários por até 25 anos.
O que exatamente o SleepFM faz
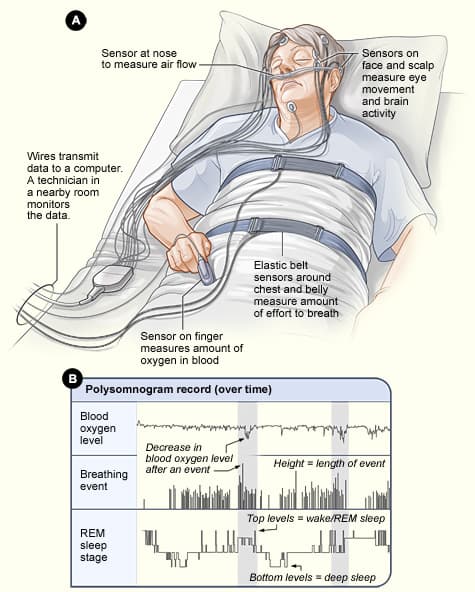
O SleepFM é um foundation model multimodal para polissonografia, o padrão ouro que registra EEG, EOG, EMG, ECG e sinais respiratórios. Em vez de focar em um único alvo, como estadiamento do sono ou apneia, ele aprende representações gerais do “idioma do sono”, com janelas de 5 segundos, e depois é ajustado para diferentes tarefas. No artigo, os autores mostram que o modelo iguala ou supera ferramentas de ponta em estadiamento e apneia, e dá o salto para predição de risco de doenças futuras.
Na métrica de sobrevivência C-index, que mede a capacidade de ordenar quem terá o evento primeiro, o SleepFM alcançou valores como 0,85 para demência, 0,89 para Parkinson, 0,81 para infarto, 0,84 para doença cardíaca hipertensiva e 0,84 para mortalidade. Esses números indicam informação clínica potencial, já que muitos modelos úteis em oncologia operam em torno de 0,7.
Por que uma única noite de sono carrega tanto sinal
Polissonografia captura horas de integração entre cérebro, coração, músculos e respiração. Em clínicas, grande parte desse oceano de dados fica subutilizada por limitações de anotação e padronização. O SleepFM atacou esse problema com uma abordagem contrastiva leave-one-out, que ensina o modelo a inferir um canal ausente a partir dos demais, robustecendo a arquitetura para montagens heterogêneas de sensores. O resultado é uma representação que resiste a variações de protocolo e generaliza para novos conjuntos.
Um ponto central do estudo é que o risco não emerge de um único traçado, e sim do desalinhamento entre sistemas. Quando cérebro parece dormir profundo enquanto o coração se comporta como se estivesse desperto, por exemplo, o modelo enxerga anomalias de coordenação que podem antecipar doença. Essa leitura de incoerência fisiológica explica por que combinações de sinais superam canais isolados.
De onde vêm os dados e por que isso importa
O treinamento reuniu quatro coortes principais, incluindo o Stanford Sleep Clinic, BioSerenity, MESA Sleep e MrOS, somando mais de 585 mil horas de sono de mais de 65 mil participantes. Para avaliar generalização, os autores ainda testaram transferência no Sleep Heart Health Study, um estudo multicêntrico com 6.441 adultos recrutados inicialmente entre 1995 e 1998, mantido fora do pré-treinamento. Essa diversidade histórica e técnica sustenta a promessa de uso em ambientes variados.
O MESA Sleep, por exemplo, incluiu polissonografia plena e actigrafia de 7 dias entre 2010 e 2012, em uma amostra multiétnica dos Estados Unidos, com dados disponibilizados pelo National Sleep Research Resource. A mistura de etnias, idades e protocolos ajuda a mitigar o viés de dados, um gargalo clássico em IA biomédica.
O que já existia e o que é novo
Modelos automáticos de estadiamento do sono evoluíram muito, com sistemas como o U-Sleep mostrando robustez a diferentes montagens e coortes. Ainda assim, o foco era tarefas de sono específicas, não a previsão ampla de doenças. O SleepFM dá um passo além, transformando o sono em um sinal de saúde longitudinal.
Mesmo na literatura recente, avanços como arquiteturas convolucionais e transformers melhoraram o estadiamento e trouxeram interpretabilidade e quantificação de incerteza. Esses trabalhos, porém, dependem de rotuladores humanos e dados menores, enquanto o SleepFM explora autoaprendizado multimodal em escala inédita para o domínio do sono.
Imagem do ambiente de polissonografia
![Montagem típica de polissonografia com sensores e traçados]
Resultados que chamam atenção em prevenção
Alguns dos melhores desempenhos do modelo apareceram em condições neurodegenerativas e cardiovasculares, como Parkinson, demência e infarto. A utilidade clínica potencial não está em diagnosticar com um exame de sono, e sim em ranquear risco com antecedência, orientando monitoramento e prevenção personalizados. No estudo, várias condições tiveram C-index 0,8 ou mais, um patamar que já orienta decisões terapêuticas em outros contextos.
Esse tipo de estratificação casa com estratégias de saúde populacional. Em coortes como a MESA Sleep, sabe-se que distúrbios do sono variam por etnia e sexo e estão associados a desfechos cardiometabólicos. Incorporar representações do sono a modelos de risco pode reduzir vieses, desde que o treinamento reflita a diversidade real.
Como aplicar hoje, com prudência
Aplicação imediata acontece em três frentes. Primeiro, pesquisa clínica, ao usar o SleepFM para gerar escores de risco e estudar mecanismos fisiológicos latentes. Segundo, triagem e priorização, ao sinalizar quem merece avaliação ampliada de fatores modificáveis, como hipertensão mascarada ou depressão incipiente. Terceiro, desenho de estudos de prevenção, ao enriquecer amostras com indivíduos de alto risco com base em um exame que muitos serviços já realizam.
Na prática clínica rotineira, o uso exige validação externa pros protocolos e populações locais. A equipe de Stanford já mostrou transferência para o SHHS, mantido fora do pré-treinamento, o que é encorajador, mas cada hospital tem peculiaridades de aquisição. É essencial validar prospectivamente antes de acoplar o modelo a fluxos de trabalho.
Limitações, riscos e perguntas em aberto
O SleepFM não é um diagnóstico. O próprio artigo e o comunicado institucional enfatizam que se trata de previsão de risco baseada em um exame único. Isso quer dizer que resultados devem ser combinados com fatores clínicos, sociais e comportamentais. Não substitui médicos, nem deve ser usado isoladamente para decisões terapêuticas.

Outra questão é a interpretabilidade. Os autores relatam técnicas especializadas para entender o que o modelo observa, mas explicações ainda são parciais. Isso é típico de foundation models biomédicos e requer camadas adicionais de explicabilidade e auditoria. Há também desafios de padronização e governança de dados, especialmente quando se considera expandir a coleta com vestíveis, que introduzem ruído e variabilidade.
Imagem de traçado do sono em estágio 2
![Traçado de polissonografia, estágio 2, com fusos do sono]
Vestíveis entram no jogo, mas com cuidado
A perspectiva é integrar sinais de polissonografia com séries temporais de vestíveis. Isso amplia cobertura e frequência, porém exige cautela. Embora vestíveis tenham valor de tendência, sua acurácia varia e depende de algoritmo, firmware e hábitos do usuário. O próprio time de Stanford sugere explorar dados adicionais para refinar predições, não substituir o padrão ouro. A ordem correta é usar vestíveis como complemento, mantendo a polissonografia como referência de verificação.
Em termos de dados, iniciativas como o National Sleep Research Resource mostram o impacto de coleções públicas bem documentadas, como MESA Sleep e SHHS, que viabilizam replicação, comparação e auditoria contínuas do desempenho do modelo. Essa infraestrutura é parte do motivo de estarmos vendo saltos qualitativos em IA do sono.
Comparando com o estado da arte em estadiamento
Ferramentas como o U-Sleep provaram robustez para estadiamento automático em adultos e têm sido investigadas até em pediatria, com resultados promissores, mas inferiores no estágio N1, tradicionalmente difícil. O SleepFM mostrou desempenho competitivo nesses marcos e vai além, mapeando risco sistêmico. Essa combinação de competência nas tarefas clássicas com generalização clínica é a diferença entre um bom classificador e uma plataforma de previsão.
O que muda para gestores e equipes clínicas
Para gestores, o ganho está em transformar um exame que já existe em sinal longitudinal. Clínicas de sono acumulam décadas de polissonografias arquivadas. Com vinculação segura a registros clínicos e protocolos de anonimização, dá para treinar e validar modelos locais, priorizar agendas, criar linhas de cuidado e medir impacto em desfechos. O estudo de Stanford usou prontuários com até 25 anos de seguimento, um diferencial para evitar atalhos espúrios.
Para equipes assistenciais, há oportunidades em prevenção cardiovascular e neurodegenerativa. Escores de risco derivados do sono podem acionar investigação de hipertensão, fibrilação atrial subclínica, comprometimento cognitivo leve ou depressão, sempre combinados com história clínica, exames laboratoriais e imagem quando indicado.
Como começar, passo a passo
- Padronize dados de polissonografia. Harmonize sampling rate, nomenclatura de canais e metadados. O artigo detalha reamostragem a 128 Hz e janelas de 5 segundos como unidade de entrada, referência útil para pipelines locais.
- Garanta governança. Crie trilhas de auditoria, anonimização e políticas de uso secundário, alinhando-se a padrões institucionais e regulatórios.
- Valide fora do treinamento. Replique a avaliação de transferência em um conjunto totalmente externo, como foi feito com o SHHS, antes de qualquer uso assistencial.
- Instrumente acompanhamento. Toda implantação deve vir com monitoramento de performance, desvios e fairness por subgrupos demográficos, inspirado pela diversidade do MESA Sleep.
Reflexões e insights
- Sono como biomarcador sistêmico. O estudo reforça que o sono não é só higiene diária, é janela para coerência entre sistemas fisiológicos. Desalinhamentos sutis podem anteceder sintomas anos antes.
- Foundation models em saúde. A estratégia de pré-treinamento auto supervisionado em multimodalidade tende a se tornar padrão para biossinais complexos, assim como já acontece em imagens médicas e texto clínico.
- Interpretação praticável. Explicabilidade perfeita talvez não seja necessária se houver governança, validação rigorosa, auditoria contínua e integração a decisões compartilhadas com o paciente.
Conclusão
A IA da Stanford mostra que uma noite de sono contém muito mais do que sonolência do dia seguinte. Com o SleepFM, representações do sono viram escores de risco para dezenas de doenças, com desempenho forte em áreas críticas como neurodegeneração e cardiologia. O caminho responsável passa por validação externa, transparência e uso combinado com avaliação clínica completa.
O avanço reposiciona o laboratório do sono como sensor de saúde populacional. A oportunidade é antecipar risco e individualizar prevenção, sem substituir médicos. Com infraestrutura de dados aberta e colaboração multidisciplinar, a próxima década deve transformar o sono em um dos sinais vitais mais informativos da medicina preventiva.
Recursos e leituras
- Artigo na Nature Medicine, publicado em 6 de janeiro de 2026.
- Comunicado de Stanford Medicine, 6 de janeiro de 2026.
- Reportagem da Longevity.Technology, 21 de janeiro de 2026.
- U-Sleep, sistema robusto de estadiamento, npj Digital Medicine, 2021.